FDA收紧新冠疫苗加强针审批标准,公众信任度引关注
AI导读:
FDA局长马蒂·马克里与疫苗监管部门负责人宣布收紧新冠疫苗加强针的审批标准,对65岁以上或高风险人群沿用现有流程,6个月以上至64岁无健康问题人群需提交随机对照临床试验结果。此举引发广泛讨论和批评,公众对疫苗的信任度下降,专家呼吁慎重考虑接种选择权。
美国食品药品监督管理局(FDA)局长马蒂·马克里与疫苗监管部门负责人维奈·普拉萨德周二在《新英格兰医学杂志》上发文,宣布收紧新冠疫苗加强针的审批标准,此举旨在提升疫苗审批的严谨性。
(来源:《新英格兰医学杂志》)
本周四,FDA的科学顾问将举行会议,讨论今年秋季新冠疫苗的构成,这一议题备受关注。
健康人群恐难获得疫苗加强针
FDA表示,针对65岁以上或6个月以上且存在健康问题(即新冠肺炎重症高风险)人群的疫苗加强针审批,将继续沿用现有流程。制药公司只需提交免疫桥接研究结果,证明疫苗的有效性。然而,对于6个月以上至64岁无健康问题的人群,制药公司需提交随机对照临床试验结果才能获批,这一变化引发了广泛讨论。
由于美国CDC对新冠重症高风险疾病的定义广泛,FDA预计,新规实施后至少1亿人仍能在现有流程下接种疫苗。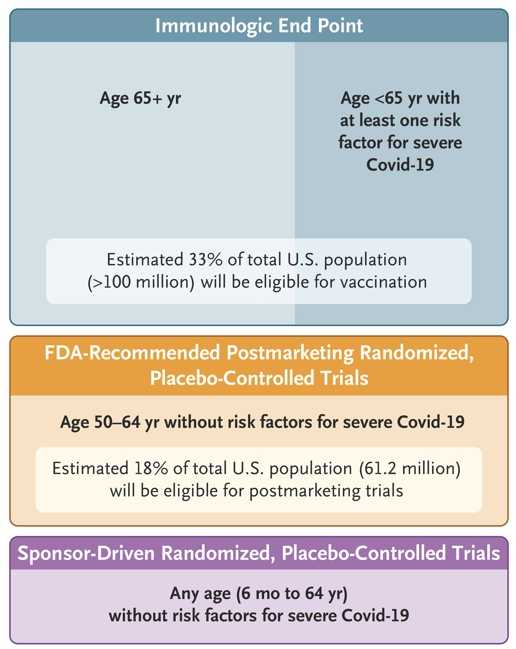
(来源:FDA)
文章指出,对于已多次接种疫苗、多次感染病毒的低风险人群,重复接种新冠疫苗的益处尚不明确。同时,欧洲多国也只建议高风险人群接种加强针。
FDA强调,针对50-64岁人群是否需要每年接种新冠疫苗的争议,将推动这一人群成为临床试验的理想对象。试验将关注有症状的新冠肺炎、重症、住院和死亡率等指标,随访期至少6个月。
此外,FDA建议开展针对儿童的研究,因为有证据表明4岁以下儿童的风险较高。
批评声四起:接种障碍引发争议
普拉萨德和马克里表示,增加健康群体的研究数据旨在恢复公众对疫苗的信任。然而,过去两年新冠疫苗加强针的接种数据不佳,公众对疫苗的信任度下降,甚至影响了其他关键免疫计划的实施。
一些专家批评称,FDA的新标准过于严苛,为健康人群设置了接种障碍,特别是那些因职业等原因面临高感染风险的人群。约翰斯·霍普金斯大学免疫研究中心主任安娜·德宾博士认为,这些政策改变毫无意义,似乎基于政治因素,将开创危险先例。
爱荷华大学医学事务副校长、美国CDC免疫接种顾问丹妮丝·贾米森博士呼吁,鉴于公众信任度下降,应慎重考虑为希望接种疫苗的人保留选择权。
(文章来源:财联社)
郑重声明:以上内容与本站立场无关。本站发布此内容的目的在于传播更多信息,本站对其观点、判断保持中立,不保证该内容(包括但不限于文字、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关内容不对各位读者构成任何投资建议,据此操作,风险自担。股市有风险,投资需谨慎。如对该内容存在异议,或发现违法及不良信息,请发送邮件至yxiu_cn@foxmail.com,我们将安排核实处理。






