CDE发布先进治疗药品征求意见稿,助力生物医药产业高质量发展
AI导读:
CDE发布《先进治疗药品的范围、归类和释义(征求意见稿)》,明确先进治疗药品范畴与归类,建立科学分类体系。这将为企业带来短期合规成本压力,但中长期将促进创新转化,提升国际竞争力,推动生物医药产业高质量发展。
近日,国家药品监督管理局药品审评中心(CDE)发布了《先进治疗药品的范围、归类和释义(征求意见稿)》(以下简称《征求意见稿》),明确了“先进治疗药品”的范畴、具体归类及分类原则。此次公开征求意见的时限为自6月10日起1个月,旨在推动生物经济高质量发展。
先进治疗领域作为“生命科学”的核心赛道,是培育未来产业的关键。然而,我国在该领域的法规界定及行业共识尚不完善,面临诸多挑战。此次《征求意见稿》聚焦于基因治疗、细胞治疗等创新技术药品,旨在建立科学的分类体系,并厘清各类型产品的监管规定。
上海市卫生和健康发展研究中心主任金春林表示,该意见稿将最前沿、最具革命性的产品纳入特殊监管范畴,并排除了传统药品。这为先进治疗药品全生命周期监管体系的建设奠定了基石,虽短期内企业可能面临合规成本压力,但中长期将促进创新转化,提升国际竞争力。
随着生物科技等前沿技术的蓬勃发展,细胞治疗、基因治疗等药品的研发数量持续增加,在疑难重症治疗方面取得突破。此次《征求意见稿》结合国际命名规范,将符合特点的一类产品命名为“先进治疗药品”(ATMPs),并详细划分了其具体类别。
先进治疗药品的界定清晰将对企业产生深远影响。短期内,企业需投入资源理解和适应新分类体系,可能增加合规成本。但中长期来看,清晰的路径和确定性将优化成本,促进创新成果转化,吸引投资,提升产业集中度。
先进治疗药品市场前景广阔。据前瞻研究院报告,2024年中国干细胞市场规模预计达265亿元,基因疗法市场规模也有望大幅增长。明确的监管路径和预期将加速创新成果转化,为产业注入发展动力,推动整个产业链的成熟,提升国际竞争力。
《征求意见稿》还体现了前瞻性和包容性,为新技术、新产品预留了空间。在实际审评中,需平衡监管与创新,以科学为本,分级分类管理,确保产品安全有效。
总而言之,《征求意见稿》及实施细则将深刻影响中国生物医药产业的未来格局,推动中国在全球尖端治疗领域占据更重要地位。
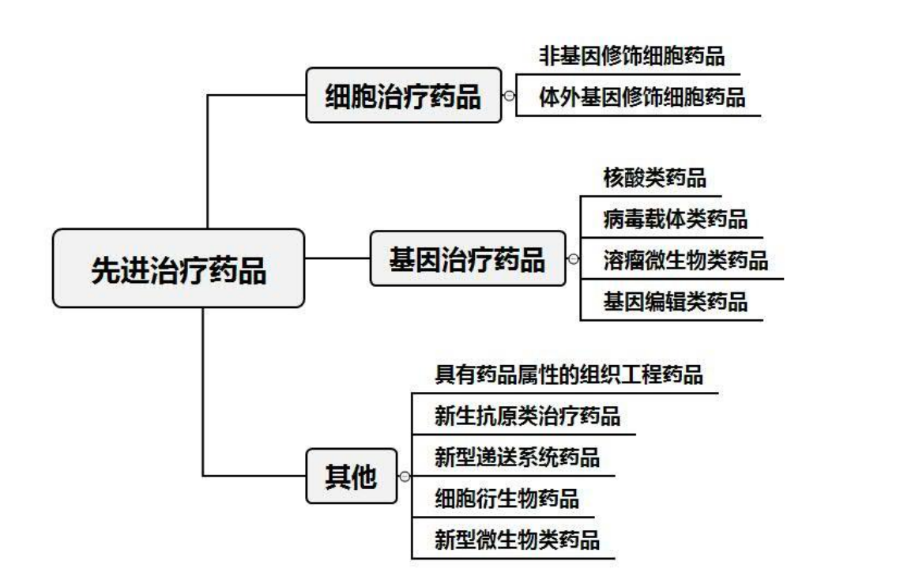
先进治疗药品具体归类及亚类示意(来源:CDE)
(文章来源:21世纪经济报道)
郑重声明:以上内容与本站立场无关。本站发布此内容的目的在于传播更多信息,本站对其观点、判断保持中立,不保证该内容(包括但不限于文字、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关内容不对各位读者构成任何投资建议,据此操作,风险自担。股市有风险,投资需谨慎。如对该内容存在异议,或发现违法及不良信息,请发送邮件至yxiu_cn@foxmail.com,我们将安排核实处理。










