科学突破:工程化细胞策略实现多器官协同抗衰
AI导读:
中国科学院动物研究所等团队成功研发出工程化人类抗衰型间充质祖细胞(SRC),并在灵长类动物模型中验证了其延缓多器官衰老的显著效果,为人类衰老干预提供全新范式,展现了广泛的抗衰效能和卓越的安全性。
随着年龄增长,干细胞储备耗竭及其引发的组织再生与稳态维持能力下降,成为机体衰老和衰老相关疾病的关键特征。然而,干细胞耗竭在衰老过程中的因果关系,以及外源性干细胞移植对延缓衰老的有效性,一直是科学界未解的难题。这一难题近日迎来了新的突破。
中国科学院动物研究所刘光慧课题组、曲静课题组,携手首都医科大学宣武医院王思课题组,成功研发出具有抗衰老、抗应激和抗恶性转化能力的工程化人类抗衰型间充质祖细胞(SRC),并在灵长类动物模型中验证了其延缓多器官衰老的显著效果,为人类衰老干预提供了全新的细胞治疗范式。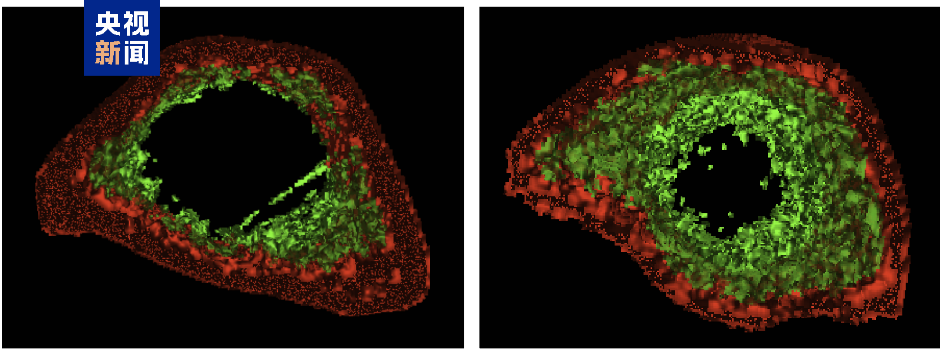
△SRC治疗有效逆转老年猴骨质疏松:对照组(左)、SRC处理组(右)
研究团队选用相当于60—70岁健康人类的老年食蟹猴作为实验对象,进行了为期44周的SRC干预研究。结果显示,多次静脉注射SRC未引发不良事件,排除了移植细胞的损伤性及致瘤风险,证实了SRC移植在非人灵长类模型中的安全性与免疫耐受性。
此外,研究全面评估了SRC对灵长类衰老模型的干预效果。结果表明,SRC移植能显著延缓猴多器官衰老进程,重建机体稳态平衡,具体表现为提升认知功能、改善多组织退行性病变、减少衰老细胞积累、增强基因组稳定性等。这一突破超越了传统“单一疾病靶向治疗”的局限,采用工程化细胞策略实现多器官协同抗衰。
该研究首次证实人类SRC能跨越灵长类种属及个体间差异,系统性地延缓多器官衰老,展现出广泛的抗衰效能和卓越的安全性。同时,系统验证了通用型基因工程干细胞在异种移植模型中的安全性和有效性,为人类异体干细胞移植的临床转化奠定了坚实基础,开辟了可规模化生产的通用型细胞干预新路径。
(文章来源:央视财经)
郑重声明:以上内容与本站立场无关。本站发布此内容的目的在于传播更多信息,本站对其观点、判断保持中立,不保证该内容(包括但不限于文字、数据及图表)全部或者部分内容的准确性、真实性、完整性、有效性、及时性、原创性等。相关内容不对各位读者构成任何投资建议,据此操作,风险自担。股市有风险,投资需谨慎。如对该内容存在异议,或发现违法及不良信息,请发送邮件至yxiu_cn@foxmail.com,我们将安排核实处理。





